שיגלוזיס
שִׁיגֵלוֹזִיס (Shigellosis), או דיזנטריה בצילרית, היא מחלה זיהומית של המעיים, הנגרמת על ידי חיידקים מהסוג Shigella ומתבטאת בדיזנטריה – שלשול דמי ורירי מלווה בכאב בטן ולעיתים חום. המחלה, אשר נפוצה בעיקר בדרום אסיה ובאפריקה שמדרום לסהרה, ושם גם עלולה לגרום לשיעורי תמותה גבוהים יותר, מועברת במחזור צואה-פה, לרוב באמצעות מים או מזון הנגועים בחיידק. כמות החיידקים הנמוכה הדרושה לגרימת מחלה, הופכת את המחלה למידבקת ביותר מבין זיהומי המעיים. האבחנה של המחלה היא על ידי זיהוי מחולל המחלה בצואה, בתרבית צואה או ב-PCR מדגימת צואה. לרוב המחלה חולפת מאליה תוך מספר ימים, אולם במחלה קשה, או במטרה למנוע התפרצויות, הטיפול כולל אנטיביוטיקה: ציפרופלוקסצין, אזיתרומיצין או צפטריאקסון.
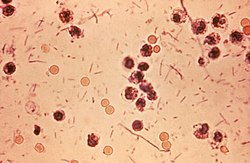 | |
| חיידקי שיגלה במשטח צואה | |
| שמות נוספים | דיזנטריה בצילרית |
|---|---|
| תחום | מחלות זיהומיות |
| שכיחות |
270 מיליון מקרים ברחבי העולם שיעור היארעות של 36.4 ל-1,000 איש |
| סיבות | חיידקים מהסוג Shigella |
| גורם |
Shigella, Shigella sonnei, Shigella boydii, Shigella flexneri, Shigella dysenteriae |
| תסמינים |
כאב בטן שלשול דמי ורירי חום |
| אבחון |
תרבית צואה PCR מצואה |
| טיפול |
צפטריאקסון קינולון אזיתרומיצין |
| פרוגנוזה | שיעור תמותה של 2.9 ל-100,000 |
| קישורים ומאגרי מידע | |
| eMedicine | article/182767 |
| DiseasesDB | 12005 |
| MedlinePlus | 000295 |
| סיווגים | |
| ICD-10 | A03 |
| ICD-11 | 1A02 |
אפידמיולוגיה עריכה
המונח דיזנטריה נטבע על ידי היפוקרטס לתיאור שלשול דמי ורירי המלווה בכאבים בצאייה, ואף שרק בשלהי המאה ה-19 נעשתה ההבחנה בין דיזנטריה בצילרית הנגרמת מ-Shigella לדיזנטריה אמבית, חלק ניכר מהתייחסות לדיזנטריה בכתבים שונים מיוחס לשיגלוזיס, נוכח ההקשר שנעשה למערכות צבאיות ולמצור, עת תנאי התברואה ירודים במיוחד.[1]
מחקר שבחן את עומס מחלת השיגלוזיס העולמי אמד בשנת 2016 את מספר המקרים ב-270 מיליון מקרים ברחבי העולם, עם שיעור היארעות של 36.4 ל-1,000 איש. מדובר בירידה בהיקף המחלה לעומת שנות ה-90 של המאה ה-20.[2] עומס המחלה הגבוה ביותר נמצא בדרום אסיה ובאפריקה שמדרום לסהרה, ושם גם שיעורי התמותה הגבוהים היותר מהמחלה. בישראל היקף התחלואה עומד על 30–60 מקרים בשנה ל-100 אלף איש, לעומת 1.6 מקרים ל-100 אלף איש באיחוד האירופי.[3]
המחלה מופיעה בעיקרה בילדים מגיל חצי שנה עד 10 שנים, כשקבוצת הגיל השכיחה ביותר היא בני שנה עד ארבע,[4] אך גם מבוגרים עלולים ללקות במחלה, בפרט אם ילדיהם חלו בה או שהם ביקרו במדינות מתפתחות. נדיר לראות תינוקות בני פחות מחצי שנה עם שיגלוזיס, ייתכן משום תזונה שמבוססת על הנקה. התפרצויות של שיגלוזיס מתוארות במעונות יום, ואף בקרב משפחות דתיות מרובות ילדים.[1]
בדומה למחלות שלשוליות אחרות, שיגלוזיס היא מחלה של תקופת הקיץ.[5] העונתיות של המחלה תוארה כבר על ידי היפוקרטס, אשר עמד על הקשר בין אביב גשום לאחר חורף שחון לבין עלייה במספר מקרי הדיזנטריה בקיץ.[1]
מגפות של שיגלוזיס עשויות להתרחש במחזורים של 20–30 שנה, ביטוי להתפתחות חסינות, אשר דועכת עם לידתם של ילדים שלא נחשפים לזן מחולל המגפה ועד להבשלת התנאים להתפרצות נוספת.[1] במחצית השנייה של המאה ה-20 התפרצו ארבע מגפות של שיגלוזיס מהזן S. Dysenteriae 1: במרכז אמריקה בסוף שנות ה-60, בדרום אסיה ובמרכז אפריקה בשנות ה-80 ובמזרח אפריקה בשנות ה-90.[4]
אטיולוגיה עריכה
- ערך מורחב – Shigella
Shigella הוא סוג מתג גראם שלילי אל-אווירני פקולטטיבי נייח וחסר קופסית ממשפחת ה-Enterobacteriaceae. הוא התגלה וזוהה כמחולל של דיזנטריה בצילרית על ידי הרופא והבקטריולוג היפני קיושי שיגה בשנת 1906, עת בודד מצואת אדם עם דיזנטריה. מספר שנים לפני כן, בודד סיימון פלקסנר חיידק דומה, אך שונה סרולוגית, מאדם אחר עם דיזנטריה שנרכשה בפיליפינים.[1]
בסוג Shigella ארבעה מינים, שמכילים יחדיו כ-40 סרוטיפים ואשר נבדלים זה מזה במאפיינים ביוכימיים וסרולוגיים: Shigella dysenteriae (קבוצה A), הנקרא גם מתג שיגה, מכיל את הסרוטיפ 1 האלים יותר, אשר נקשר בהתפרצויות רחבות-היקף ותמותה במדינות מתפתחות. Shigella flexneri (קבוצה B) הוא הזן האנדמי במדינות המתפתחות באסיה ובאפריקה. Shigella boydii (קבוצה C) אנדמי לתת-היבשת ההודית. Shigella sonnei (קבוצה D) הוא הזן אנדמי בעולם המערבי.[6] בישראל 95% ממקרי השיגלוזיס המאובחנים נגרמים מזן זה, בעוד היתר נגרמים מ-S. flexneri.[7]
לחיידקי ה-Shigella קרבה גנטית לזן Enteroinvasive E. coli (EIEC), מחולל נוסף של דיזנטריה בצילרית. חיידקים אלה חולקים גורמי אלימות משותפים, אשר חלקם כרומוזומליים וחלקם מועברים אופקית.
פתוגנזה עריכה
העברה עריכה
חיידק ה-Shigella מועבר מאדם לאדם במחזור צואה-פה. החיידק יכול לעבור, למשל, בין ידיים לא רחוצות, כשמספר החיידקים הנמוך, לעיתים אף פחות מ-100,[8] הנחוץ לגרימת מחלה, הופך את שיגלוזיס למחלה השלשולית החיידקית המידבקת ביותר. הדבר מסביר מדוע התפרצויות עלולות להתרחש בקרב אוכלוסיות המתגוררות בצפיפות, דוגמת מחנות צבא, בתי כלא, מוסדות לחוסים ומשפחות מרובות ילדים.[1][4] באופן דומה, צריכה של מזון או מים מזוהמים בחיידק הם מקור לרכישת שיגלוזיס, כשהתפרצויות עשויות להתרחש כאשר מקור מזון או מים משותף, דוגמת באר מים, מזדהם בצואה נגועה בחיידק. בנוסף, מתוארות גם התפרצויות של שיגלוזיס עמיד לאנטיביוטיקה בקרב גברים המקיימים יחסי מין עם גברים.[9] זבוב הבית נקשר אף הוא בהעברה של שיגלוזיס, בפרט באזורים טרופיים, נוכח העלייה בשיעור הדיזנטריה כשאוכלוסיית הזבובים בשיאה, הזיקה של זבוב זה לצואת אדם, הבידוד של חיידקי Shigella מזבובים בשילוב עם המזרע הנמוך הדרוש לגרימת מחלה, והפחתת שיעורי הדיזנטריה בעת הדברת זבובים סביבתית.[10]
חדירה לרירית המעי עריכה
חיידקי ה-Shigella העמידים לתנאי החומציות שבקיבה,[11] עושים את דרכם לאחר הבליעה לעבר המעי הדק, ותוך 12 שעות מתרבים ומגיעים לריכוזים של עשרות מיליונים עד מיליארד תאים למ"ל תוכן מעי. בתוך מספר ימים החיידקים עוזבים את המעי הדק ומתיישבים במעי הגס. כפי שעולה ממחקר שבחן את המראה הקולונוסקופי של שיגלוזיס, ככל שמתקדמים במעי הגס לעבר החלחולת, כך המעי מעורב יותר במחלה, עם מעורבות של 100% במעי העקול והחלחולת, ושיעור הולך ויורד עד ל-15% במעי הגס העולה.[12]
במעי הגס החיידקים חודרים לתאי רירית המעי, לרבות תאי האפיתל, המקרופאגים ולתאי M. לצורך החדירה הם עושים שימוש במערכת הפרשה מסוג III, המזריקה חלבונים חיידקיים, בהם רעלנים ומשרי אפופטוזה, לתא הרירית. החיידקים מתרבים בתוך תאי המעי ועוברים להדביק תאים סמוכים בתהליך תלוי אקטין, תוך שהם גורמים להרס של התאים ומעוררים דלקת. זיהום זה מוגבל לרקמת הרירית בלבד, ומעבר של החיידק לזרם הדם הוא נדיר.[8]
רעלנים עריכה
בעוד ארבעת המינים של Shigella נושאים על גבי פלזמיד את הגן לרעלן ShET2 (אנטרוטוקסין שיגלה 2), הזן S. flexneri 2a נושא בכרומוזום את הגן ל-ShET1 (אנטרוטוקסין שיגלה 1), ואילו הזן S. dysenteriae 1 מייצר את רעלן השיגה STx, הדומה לרעלן המופרש מ-Enterohemorrhagic E. coli ונקשר בהתפתחות תסמונת המוליטית-אורמית. רעלנים אלה גורמים להפרשת מים ואלקטרוליטים לחלל המעי.
דלקת עריכה
אף שהחיידקים גורמים לדיכוי הפרשת פפטידים אנטימיקרוביאליים, ובכך מצליחים להתחמק ממערכת החיסון, בסופו של דבר, הרס הרירית מעורר תגובה חיסונית תאית והומורלית, עם עלייה ברמות ציטוקינים ככל שהמחלה קשה יותר.[8] הנזק הרקמתי והתגובה הדלקתית מתארגנים לכדי מורסות זעירות, המתמזגות זו עם זו לכדי מורסות גדולות יותר, שמתקלפות מהרירית ויוצרות כיבים ברירית.
תסמינים וסימנים עריכה
תקופת הדגירה של המחלה היא 1–4 ימים.[4] לאחר מכן, שלב ריבוי החיידק במעי הדק מביא לתסמינים של כאב בטן עוויתי וחום, המתועד בכשליש מהמקרים. לאחריהם מופיע שלשול מימי בנפח גבוה. עם מעבר החיידקים למעי הגס, החום יורד אך תדירות השלשולים עולה במקביל לירידה בנפח, והצואה עצמה עשויה להפוך לדמית (40% מהמקרים) ורירית (50% מהמקרים), עם דחיפות לצאייה ודחף ריק (טנזמוס, התחושה שצאייה קרֵבה מבלי שיוצא תוכן).[1]
הממצאים בבדיקה הגופנית עשויים לכלול חום גבוה, רגישות בבטן תחתונה וניע ער. ביצוע בדיקה רקטאלית יפיק כאב, והרירית תיראה גדושה ופריכה, עם ריבוי הפרשות ריריות ואזורי דמם כתמי. התכייבות של רירית החלחולת יכולה להיראות לאחר מספר ימי מחלה. באנשים עם שלשולים מרובים, תיתכן צניחת חלחולת.[1]
בדיקות עזר עריכה
בספירת דם מלאה ניתן לראות לעיתים לויקוציטוזיס, או לחלופין לויקופניה, עם ריבוי צורות צעירות (סטייה שמאלה). הסתכלות מיקרוסקופית ישירה על משטח צואה צבוע במתילן בלו תראה ריבוי תאי דם לבנים, בעיקר נויטרופילים. ריבוי תאי הדם הלבנים בצואה מעיד על דלקת מפושטת של המעי הגס. רמות לקטופרין בצואה היא בדיקה רגישה יותר למידת הדלקת ברירית המעי, ובמרבית מקרי שיגלוזיס היא חיובית.
זיהוי מתג ה-Shigella בצואה מתבצע בראש ובראשונה בעזרת תרבית, בפרט בשלבי המחלה הראשונים, כאשר עומס החיידקים בצואה גבוה. בשלבי ההחלמה ריכוז החיידקים בצואה יורד במספר סדרי גודל. העברת הדגימה בהקדם למעבדה תביא לשיעור זיהוי גבוה יותר, שכן ככל שדגימת הצואה עומדת בטמפרטורת החדר, חלה ירידה במספר התאים החיוניים. לצורך זיהוי החיידק נזרעת הדגימה על שני מצעי גידול שונים לפחות. האחד כולל מעכבים מעטים של חיידקים גראם שליליים, דוגמת אגר מקונקי, והשני סגולי יותר עם יורת מעכבים, דוגמת מצע שיגלה–סלמונלה. מושבת החיידק מתאימה לחיידקים שאינם מפרקים לקטוז.[1]
בנוסף, בדיקת PCR עשויה אף היא לזהות את החיידק בצואה, אלא שהגן הנבדק משותף ל-EIEC, ולכן הבדיקה אינה יכולה להבדיל בין שני החיידקים הדומים הללו. במכוני מחקר משתמשים גם בצביעות פלואורסצנטיות תחת המיקרוסקופ.[1] רמת הנוגדנים נגד שיגלה עולה בדם בשלב ההחלמה, ואף שמידת העלייה נמצאת במתאם לחומרת המחלה, כלי סרולוגי זה משמש בהקשרים אפידמיולוגיים.[1]
אבחנה עריכה
החשד האבחנתי לשיגלוזיס עולה באנשים המתייצגים עם שלשול חריף המלווה בתסמינים סיסטמיים, בפרט אם השלשול נמשך למעלה מיומיים, החום גבוה, יש דם או ריר בצואה, או כאשר יש הדבקה בתוך המשפחה בהפרש של עד שלושה ימים בין המקרים.
תרבית צואה היא מדד הזהב לאבחנה. עם זאת, שיטות PCR, לרבות PCR המכוון למספר מחוללים בו־זמנית, הולכות ותופסות נתח נרחב יותר באבחנה של שיגלוזיס, שכן רגישותן וסגוליותן גבוהות מאוד ביחס לתרבית צואה (96% ו-99%, בהתאמה, עבור זיהוי Shigella או EIEC[13]), והזמן לקבלת תשובה מתקצר למספר שעות, תוך הפחתת העלויות הכוללות של הבירור והטיפול. החסרונות של השיטות המולקולריות הללו הוא בחוסר היכולת שלהן להבחין בין Shigella ל-EIEC, נוכח הגן הזהה שמאותר בבדיקה, ובכך שאינן נותנות מידע על עמידות לאנטיביוטיקה. משום כך, לאחר זיהוי של Shigella או EIEC בבדיקה מולקולרית של צואה, מתבצע וידוא של התוצאה על ידי תרבית לצרכים אפידמיולוגיים ולצורך קבלת מידע על עמידות.[1]
באבחנה המבדלת לשיגלוזיס נמצאות סיבות אחרות לשלשול, ובפרט לדיזנטריה ולדלקת הקיבה והמעיים, דוגמת אמביאזיס. מאחר ששיגלוזיס היא מחלה חריפה, סיבות כרוניות יותר לשלשול דלקתי עם דם וריר, הן פחות סבירות אם כי לא נשללות על הסף.
טיפול עריכה
אף על פי ששיגלוזיס אינה גורמת בדרך כלל לאובדן נוזלים ואלקטרוליטים משמעותי בשלשול, בגילאי הקצה ניכרת לעיתים התייבשות, הניתנת לטיפול באמצעות החזרי נוזלים ומלחים. החזרי הנוזלים ניתנים דרך הפה, אלא אם ישנן הקאות מרובות או שהאדם במצב כללי ירוד, שאז הם ניתנים בעירוי.
מאחר שברוב המקרים שיגלוזיס היא מחלה החולפת מאליה, ומאחר שהשימוש העודף באנטיביוטיקה עלול לברור זנים עמידים, טיפול אנטיביוטי ניתן לאנשים עם מחלה בדרגת חומרה קשה,[14] כגון אנשים שמחלתם מחייבת אשפוז, אנשים עם תיעוד החיידק בדם ואנשים עם סיבוכים אחרים של המחלה. כמו כן, אנטיביוטיקה ניתנת לאנשים שיש להם גורמי סיכון לפתח מחלה קשה, ובפרט אנשים עם דיכוי חיסוני וקשישים. בנוסף, במטרה למנוע התפרצות, טיפול אנטיביוטי ניתן לאנשים העובדים עם מזון, לדיירי בתי אבות ומוסדות אשפוז כרוני ולאנשים העובדים במעונות יום. אוכלוסיות אלו יקבלו טיפול גם אם יאותרו כנשאים ללא מחלה גלויה.[1]
בשל שיעורי עמידות לאנטיביוטיקה הולכים ועולים, הטיפול האמפירי מביא בחשבון את גורמי הסיכון ל-Shigella עמידה, כך שבאנשים ללא גורמי סיכון ציפרופלוקסצין היא תרופת הבחירה, בעוד שבאנשים עם גורמי סיכון ניתן לטפל בצפלוספורין מדור שלישי, דוגמת צפטריאקסון. גורמי הסיכון הם שהות בדרום-מזרח אסיה ובאפריקה, גברים המקיימים יחסי מין עם גברים ו-HIV.[1]
הקווים המנחים של החברה האמריקאית למחלות זיהומיות ממליצים כקו ראשון על טיפול אנטיביוטי באזיתרומיצין, ציפרופלוקסצין או צפטריאקסון לטיפול בשיגלוזיס.[14] בנוסף, במקרה של ריכוז מעכב מזערי של 0.12 מיקרוגרם למ"ל ומעלה עבור ציפרופלוקסצין, מנחים המרכזים לבקרת מחלות ומניעתן על הימנעות ממתן התרופה, גם אם הדיווח של המעבדה מזהה את החיידק כרגיש.[15] חלופות אפשריות הן טרימתופרים/סולפמתוקסזול. שיותר ויותר זנים הפכו עמידים אליה, ואמפיצילין.[14] משך הטיפול המקובל הוא שלושה ימים.[1]
הסיכון לפתח תסמונת המוליטית-אורמית הקיים בזנים המפרישים את רעלן השיגה עולה לאחר טיפול אנטיביוטי. משום כך, זיהוי של חיידק המפריש את הרעלן בצואה יביא להימנעות מטיפול אנטיביוטי.
הטיפול בתרופות עוצרות עלול להחמרת חדירת החיידק לרירית המעי, ועל כן נחשב כלא מועיל. אולם, אם ניתן יחד עם אנטיביוטיקה, הוא עשוי לקצר את משך השלשול.[16]
פרוגנוזה וסיבוכים עריכה
באנשים עם מערכת חיסונית כשירה שיגלוזיס היא מחלה חולפת מאליה, וגם בהיעדר טיפול אנטיביוטי היא נמשכת בין מספר ימים לחודש, כשהממוצע עומד על שבעה ימים. עם זאת, מבין מחלות השלשולים הזיהומיות, היא מביאה יותר אנשים לכדי אשפוז. מחלה קשה יותר נצפית בילדים בתת-תזונה, במדוכאי חיסון ובקשישים, אז גם הסיכון לתמותה עולה.[4]
הסיבוכים אינם שכיחים וכוללים: התייבשות חמורה, פרכוסי חום בילדים, אלח דם, דלקת ריאות, דלקת לחמית וקרנית ודלקת פקעיות הכליה כתוצאה משקיעת מכלולי חיסון.
סיבוכים המופיעים לאחר חלוף הזיהום כוללים: תסמונת מעי רגיז המופיעה ב-4% מהמקרים במדינות מפותחות, דלקת מפרקים ראקטיבית, ובחיידקים המפרישים את רעלן השיגה תסמונת המוליטית-אורמית.[4]
הזן S. Dysenteriae 1 גורם בדרך כלל למחלה קשה יותר, ובעת התפרצויות כאשר לא מטופל, כרוך בשיעורי תמותה של עד 20%.[1]
מניעה עריכה
מניעה סביבתית עריכה
בדומה לזיהומים אחרים העוברים במחזור צואה-פה, הבטחת גישה למי שתייה נקיים היא צעד מהותי בצמצום ההיקף של שיגלוזיס, בפרט במדינות מתפתחות עם תשתיות תברואה לקויות. באופן דומה, הכלרת מים היא צעד נוסף בהפחתת שיעור הזיהומים החיידקיים של מערכת העיכול העוברים במים. הדברת מזיקים מסייעת אף היא בצמצום אוכלוסיית החרקים היכולים להעביר את המחלה.
ברמת הפרט, שמירה על היגיינה אישית עם רחצת ידיים תכופה ויעילה ושמירה על בטיחות המזון, לרבות הרחקת אנשים משלשלים מהכנת מזון ובישול מזון ואחסנתו בתנאי קירור נאותים, עשויים לצמצם התפרצויות של המחלה. במקומות בעלי פוטנציאל הדבקה גבוה, כמו מעונות יום ומוסדות לטיפול כרוני, וידוא הכחדת החיידק על ידי תרבית שלילית בסיום טיפול אנטיביוטי עשויה לצמצם את הסיכון להתפרצות. בעולם המתפתח הנקה היא אמצעי להפחתת סיכויי הדבקת תינוקות בשיגלוזיס.
חיסון עריכה
ניסיונות לייצור חיסון לשיגלוזיס טרם הבשילו לכדי פיתוח תרכיב. עוד בשנת 1919 ניסח האימונולוג אלכסנדר בזרדקה את הרעיון שלפיו החסינות בפני דיזנטריה בצילרית, הנרכשת לאחר מחלה, היא תוצאה של ריגוש רירית המעי למתגי הדיזנטריה, וכי לנוגדנים בנסיוב תפקיד מזערי, אם בכלל, בהקניית חסינות. אחד הניסיונות המוצלחים יותר היה מתן של זנים חיים מוחלשים של שיגלה לאוכלוסיית חיילים בצבא יוגוסלביה ולילדים באזורים היפראנדמיים. החיסון ניתן במספר מנות והצליח למנוע מחלה, אך לא למנוע נשאות.[1]
ראו גם עריכה
קישורים חיצוניים עריכה
- אלעד נוי, נדב אור, יונתן בוקסמן, פיתוח והערכת חיסונים נגד שיגלוזיס בחיל הרפואה, הרפואה הצבאית, כרך 6, חוברת 4, אוקטובר 2009
הערות שוליים עריכה
- ^ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Herbert L. DuPont, Pablo C. Okhuysen, 224 - Bacillary Dysentery: Shigella and Enteroinvasive Escherichia coli, Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases (Ninth Edition), edited by Bennett John E., Dolin Raphael, Blaser Martin J., 2020, Pages 2737-2742.e3, ISBN 978-0-323-48255-4, http://dx.doi.org/10.1016/B978-0-323-48255-4.00090-4.
- ^ Khalil, I. A., Troeger, C., Blacker, B. F., Rao, P. C., Brown, A., Atherly, D. E., … Reiner, R. C. (2018). Morbidity and mortality due to shigella and enterotoxigenic Escherichia coli diarrhoea: the Global Burden of Disease Study 1990–2016. The Lancet Infectious Diseases. doi:10.1016/s1473-3099(18)30475-4
- ^ מערכת דוקטורס אונלי, מומחים: שיעור הזיהומים כתוצאה מחיידקים במזון בישראל - גבוה מזה בארה"ב ובאירופה, באתר DoctorsOnly, 18 באוגוסט 2016
- ^ 1 2 3 4 5 6 Kotloff KL, Riddle MS, Platts-Mills JA, Pavlinac P, Zaidi AKM. Shigellosis. Lancet. 2018 Feb 24;391(10122):801-812. doi: 10.1016/S0140-6736(17)33296-8.
- ^ מערכת וואלה!, גן סגור: מהו חיידק השיגלה ולמה הוא מסוכן?, באתר וואלה!, 29 בספטמבר 2016
- ^ Yang F, et al. Genome dynamics and diversity of Shigella species, the etiologic agents of bacillary dysentery. Nucleic Acids Res. 2005 Nov 7;33(19):6445-58. doi: 10.1093/nar/gki954.
- ^ הרעלת מזון: שיגלה, באתר משרד הבריאות, 8 בפברואר 2021 (עדכון: 14 במרץ 2023)
- ^ 1 2 3 Sansonetti, P. J. (2001). Rupture, invasion and inflammatory destruction of the intestinal barrier byShigella, making sense of prokaryote–eukaryote cross-talks. FEMS Microbiology Reviews, 25(1), 3–14. doi:10.1111/j.1574-6976.2001.tb00569.x
- ^ Bowen A, Grass J, Bicknese A, et al. Elevated Risk for Antimicrobial Drug–Resistant Shigella Infection among Men Who Have Sex with Men, United States, 2011–2015. Emerging Infectious Diseases. 2016;22(9):1613-1616. doi:10.3201/eid2209.160624.
- ^ Levine, O. S.; Levine, M. M. (1991). Houseflies (Musca domestica) as Mechanical Vectors of Shigellosis. Clinical Infectious Diseases, 13(4), 688–696. doi:10.1093/clinids/13.4.688
- ^ Carlton A.W. Evans; Robert H. Gilman; G.H. Rabbani; Guillermo Salazar; Akbar Ali (1997). Gastric acid secretion and enteric infection in Bangladesh., 91(6), 681–685. doi:10.1016/s0035-9203(97)90523-x
- ^ Speelman P, Kabir I, Islam M: Distribution and spread of shigellosis: a colonic study. J Infect Dis 1984; 150: pp. 899-903.
- ^ Buss SN, Leber A, Chapin K, et. al.: Multicenter evaluation of the BioFire FilmArray gastrointestinal panel for etiologic diagnosis of infectious gastroenteritis. J Clin Microbiol 2015; 53: pp. 915-925
- ^ 1 2 3 Shane AL, Mody RK, Crump JA, Tarr PI, Steiner TS, Kotloff K, Langley JM, Wanke C, Warren CA, Cheng AC, Cantey J, Pickering LK. 2017 Infectious Diseases Society of America Clinical Practice Guidelines for the Diagnosis and Management of Infectious Diarrhea. Clin Infect Dis. 2017 Nov 29;65(12):e45-e80. doi: 10.1093/cid/cix669.
- ^ CDC Recommendations for Diagnosing and Managing Shigella Strains with Possible Reduced Susceptibility to Ciprofloxacin, CDC, 18 באפריל 2017
- ^ Murphy GS, Bodhidatta L, Echeverria P, et. al.: Ciprofloxacin and loperamide in the treatment of bacillary dysentery. Ann Intern Med 1993; 118: pp. 582-586.
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.