Streptococcus mutans
Streptococcus mutans (בקיצור: S. mutans, בתעתיק לעברית: סטרפטוקוקוס מוטנס) הוא חיידק בעל תצורה נקדית-אליפטית במקצת, גראם-חיובי, אל-אווירני פקולטטיבי (שיכול לגדול בנוכחות חמצן או באווירה עניה בחמצן ועשירה בדו-תחמוצת הפחמן). חיידקים אלו נפוצים מאוד בחלל הפה, והם נחשבים לגורמים העיקריים לעששת שיניים[1]. החיידק שייך לסוג Streptococcus ותואר לראשונה על ידי Kilian Clarke בשנת 1924[2], שבודד את החיידקים מנגעי עששת בבני אדם. החיידק Streptococcus mutans הוא מין אחד מתוך קבוצת מינים דומים הנקראת mutans streptococci[3], ואליה שייכים גם Streptococcus sobrinos הנפוץ אף הוא בבני אדם, ומינים נוספים הנפוצים יותר בחיות.
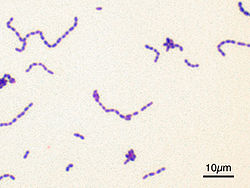 שרשראות חיידקי S. mutans מבעד למיקרוסקופ אור
שרשראות חיידקי S. mutans מבעד למיקרוסקופ אור
לאחר צביעת גראם (הגדלה X100) | |
| מיון מדעי | |
| ממלכה: | חיידקים אמיתיים |
| מערכה: | Firmicutes |
| מחלקה: | Bacilli |
| סדרה: | Lactobacillales |
| משפחה: | Streptococcaceae |
| סוג: | Streptococcus |
| מין: | Streptococcus mutans |
| שם מדעי | |
כללי עריכה
חיידקי S. mutans נפוצים מאוד בחלל הפה, והם נחשבים לגורמים העיקריים לעששת שיניים[1][4]. החיידק תואר לראשונה על ידי Kilian Clarke בשנת 1924[2], אשר בודד את החיידקים מנגעי עששת בבני אדם. החיידק Streptococcus mutans הוא מין אחד מתוך קבוצת מינים דומים הנקראת mutans streptococci[3], ואליה שייכים גם Streptococcus sobrinos הנפוץ אף הוא בבני אדם, ומינים נוספים הנפוצים יותר בחיות.
מחקרים רבים התייחסו וזיהו את S. mutans כגורם העששת העיקרי. לכך יש מספר סיבות – ביניהן – ניתן לבודד חיידקים אלו כמעט מכל נגע עששתי. בנוסף, חיידק זה הצליח לגרום לעששת בחיות מעבדה שקיבלו דיאטה עשירה בסוכרוז. לחיידקים אלו יש תכונות כמו אצידוגניות (יצירת חומצות) ואצידוריות (יכולת לגדול בנוכחות חומצה) – מה שחשוב לגבי תהליך העששת. כמו כן – הם יוצרים גלוקנים - פולימרים בלתי מסיסים של מולקולות גלוקוז, שהן מתוצרי הפירוק סוכרוז, מה שעוזר להם להיצמד לשיניים, זה לזה ולחיידקים אחרים[1]. עם זאת, לא תמיד הם מתגלים במספרים גבוהים בנגעים עששתיים, ואז יש תפקיד לחיידקים אצידוגניים ואצידוריים נוספים מסוג – non-mutans streptococci, כמו: Lactobacilli, Actinomyces, ו-Bifidobacterium[5].
אקולוגיה עריכה
בחלל הפה יש כמה מאות מינים של חיידקים, מהם כמה עשרות מינים של סטרפטוקוקים, כאשר לכל אחד מהם העדפות התיישבות שונות והתאמות מיוחדות לנישות השונות בחלל הפה. רק מיעוטם יכולים לגרום לעששת, כשהעיקרי ביניהם S. mutans. החיידקים הנצמדים למשטחי השיניים יוצרים את הרובד הדנטלי, הנקרא גם הביופילם הדנטלי (Dental Plaque/Dental Biofilm). זהו רובד המורכב מחיידקים רבים ותוצריהם, כאשר S. mutans מהווה חלק מרובד זה. הרב-סוכרים (הפוליסכרידים) כמו הגלוקנים השונים, הם תוצרי החיידקים ברובד, שעוזרים להם להיצמד זה לזה ולמשטחי השיניים. כאשר תדירות צריכת הסוכרים גבוהה, התנאים בפה חומציים למשך זמן ארוך בשל פירוק הסוכרים ויצירת חומצות, מה שגורם לתנאים מועדפים לאוכלוסיית החיידקים מפרקי הסוכר ויוצרי החומצות. דבר זה עלול לגרום להפרת האיזון האקולוגי הקיים באוכלוסיית החיידקים של חלל הפה, דבר אשר מוביל לתחילת התהליך העששתי.
מחקר משנות ה-70 מצא שלחיידקי S. mutans יש העדפה ברורה למשטחי השיניים בפה, והם היוו כ-40% מכלל הסטרפטוקוקים שהתיישבו בחרירים והחריצים בשיניים. מכלל החיידקים השוכנים בחלל הפה, רק כ-2%-9% מחיידקי S. mutans נמצאו על הרקמות הריריות של הלחיים[6].
מעורבות בעששת עריכה
ל-Streptococcus mutans וגם ל-Streptococcus sobrinos, השייכים לקבוצת ה-mutans streptococci, יש תפקיד מרכזי במעורבות בעששת שיניים. זאת מכיוון שחיידקים אלו מפרקים סוכרים (בייחוד סוכרוז), ובחילוף החומרים שלהם נוצרת חומצה לקטית. כך מתאפשרת הדה-מינרליזציה (המסת מינרלים כמו הסידן) מתוך זגוגית השן, ומתחיל התהליך העששתי[7]. הסוכרוז משמש לחיידקים אלו לייצור של הפוליסכרידים המופרשים אל מחוץ לתא החיידק - הגלוקנים השונים, בעזרת האנזים גלוקן סוכראז (שנקרא גם גלוקוזיל טרנספראז)[8], בתגובה הבאה:
סוכרוז (=גלוקוז+פרוקטוז) ← גלוקן (=פולימר גלוקוז) + פרוקטוז
סוכרוז הוא הסוכר היחיד שהחיידק S. mutans יכול לנצל כדי לייצר את הגלוקנים הדביקים. עם זאת, חיידקי S. mutans יכולים לפרק גם סוכרים רבים אחרים, כמו גלוקוז, פרוקטוז, לקטוז ועוד, ואפילו במידה מסוימת סוכרי כוהלים שבהם משתמשים כתחליפי סוכר במוצרי מזון שונים (כמו סורביטול ומניטול). קסיליטול (Xylitol) הוא תחליף הסוכר היחיד שהחיידקים לא יכולים לפרק, ויש לו גם השפעה מעכבת על גידולם בתרחיף. אך בניגוד לממצאים לגבי השפעת קסיליטול על חיידקים בתרחיף (פלנקטוניים), שגרם לעיכוב גידול על ידי יצירת מעגל גליקוליזה עקר, כשהחיידקים היו בביופילם (כמו מצבם על השיניים) ולא בתרחיף לא הייתה לקסיליטול השפעה מעכבת המוזכרת לעיל[9]. מחקרים רבים נעשו לגבי המעורבות של S. mutans ו-mutans streptococci נוספים בעששת. המחקרים הראשונים נעשו בתחילת שנות ה-60, במודלים של אוגרים וחולדות על ידי Keyes ,Fitzgerald[10] וחוקרים נוספים, שהראו כי ניתן להדביק בעששת חיות שהן נטולות חיידקים (germ-free) בעזרת S. mutans[1]. רק אחרי כעשור, הושוו הממצאים לתגליות של Clarke בשנות העשרים בבני אדם[2]. בנוסף לתכונות שצוינו לעיל, הסיבות שבגללן הסיקו שיש ל-S. mutans מעורבות בעששת קשורות למספר עובדות שנמצאו במחקרים מדעיים. נמצאה קורלציה גבוהה בין נוכחות של החיידק במספרים גבוהים במקרי עששת בילדים ובמבוגרים, ולהפך - מספרים נמוכים (או שהחיידק כלל לא נמצא) במקרים שאין עששת. עובדה נוספת הקשורה למעורבות בעששת, היא היכולת של חיידקי S. mutans לשרוד ולגדול בתנאים חומציים (ב-pH נמוך), הנוצרים בעקבות יצירת החומצות מפירוק הסוכרים[1].
יכולת יצירת עששת (פוטנציאל קריוגני) עריכה
המעורבות של S. mutans בעששת קשורה במספר תכונות שהופכות אותו לחיידק הקריוגני (יוצר העששת) העיקרי. כדי שחיידק יוכל לגרום לעששת שיניים, עליו להיצמד למשטחי השיניים - ואת זאת עושה S. mutans בעזרת מולקולות אדהזיה חלבוניות שנמצאות על פני שטח החיידק וקרויות "אנטיגן" I/II[11]. מולקולה "אנטיגן" I/II, קיימות בכל חיידקי קבוצת ה-mutans streptococci והוא נצמד לגליקופרוטאין מסוים ברוק, הנקרא אגלוטינין, או בשמו המדעי - gp-340 (גליקופרוטאין במשקל מולקולרי של kDa340)[1]. האגלוטינין שברוק מצפה את משטחי השיניים ומשמש כרצפטור ל-Antigen I/II, וכך נצמדים החיידקים בעזרתו לשיניים.
תכונה נוספת של S. mutans שעוזרת לו בהיצמדות לשיניים ולרובד החיידקים שעל השיניים, היא ייצור הרב-סוכרים החוץ תאיים. תרכובות אלו נוצרות על ידי פירוק הסוכרים בעזרת האנזימים המתאימים, כמו האנזים גלוקן סוכראז, היוצר גלוקנים בלתי מסיסים המשמשים כחומרי דבק. S. mutans מייצר גם פרוקטנים, שהם פולימרים של פרוקטוז, בעזרת האנזים פרוקטן סוכראז (הנקרא גם פרוקטוזיל טרנספראז)[8].
בנוסף לייצור והפרשה של רב-סוכרים חוץ תאיים, S. mutans גם מייצרים רב-סוכרים תוך-תאיים מהסוכרים, לשימוש ואגירה בציטופלסמה של החיידק. הרב-סוכרים התוך-תאיים עוזרים לחיידקים לשרוד גם בתנאים של חוסר מקור מזון חיצוני.
לחיידקים אלו יש גם אנזים בשם Phosphoenolpyruvate sugar:phosphotransferase, שתפקידו לזרז קליטת סוכרים שונים. זוהי תכונה קריטית לניצול הסוכרים לגידול החיידקים ולייצור החומצות הגורמות לתהליך העששת.
תכונה נוספת התורמת לפוטנציאל הקריוגני של החיידק היא עמידותו לתנאים חומציים שהם קטלניים לרוב החיידקים האחרים בפה. אחד המנגנונים המקנה לחיידקים את העמידות לחומצות הוא אנזים מסוג ATPase הנמצא בקרום התא של החיידק ובציטופלסמה שלו. אנזים זה משתמש במולקולת ה-ATP על מנת לשאוב יוני מימן (שהם הגורמים לחומציות) מתוך תא החיידק החוצה וכך להוריד את רמת החומציות בתוכו[1].
המופע הראשון עריכה
מחקרים אפידמיולוגיים הראו שבילדים מופיע S. mutans לראשונה עם בקיעת השיניים הראשונות. מקור החיידקים - ככל הנראה מהאם (או מהגורם הקרוב ביותר המטפל בילד), על ידי הדבקה מהרוק. ילדים יכולים גם להידבק בחיידק מילדים אחרים במסגרות הטיפוליות השונות בהן הם נמצאים[12][13][14].
מעורבות במחלות לב וכלי דם עריכה
חלק מהסטרפטוקוקים האוראליים וביניהם S. mutans, נמצא קשור למחלות סיסטמיות כמו מחלות לב וכלי דם (מחלות קרדיו-וסקולריות). חיידקים אלו בודדו גם במקרים של זיהום חיידקי בדם (בקטרמיה), וכן בדלקת זיהומית של פנים הלב[15]. הגעת החיידקים למחזור דם עלולה להתרחש במהלך טיפולי שיניים חודרניים שונים – כמו עקירת שיניים או טיפולי שורש. דרך הדם – החיידקים יכולים להגיע במהירות לאיברים כמו הלב ולגרום לדלקת זיהומית של פנים הלב, מחלה שעלולה להיות קטלנית[16].
גידול החיידקים במעבדה עריכה
ניתן לבודד את חיידקי S. mutans מהפה ולגדלם במעבדה על מצע אגר סלקטיבי מסוג Mitis Salivarius Agar. המצע מכיל את האנטיביוטיקה Bacitracin (המעכבת את יצירת הדופן הפפטידוגליקנית של חיידקים הרגישים לה) וגורמים סלקטיביים נוספים - כמו סוכרוז בריכוז גבוה (10-20%), הצבעים Crystal violet ו-Trypan blue, וכן Potassium Tellurite. חיידקי S. mutans יכולים לגדול על המצע בנוכחות החומרים הנ"ל, אבל חיידקים אחרים מעוכבים במצע זה[17]. לאחר הדגרת המצע לצורך מתן זמן לגידול, מושבות החיידקים המתקבלות נראות כמו סלעים או גבישים כחולים (ראו תמונה).
מניעה וטיפול עריכה
היגיינה עריכה
הדרך היעילה ביותר להקטנת רמות החיידקים על גבי השיניים היא שמירת היגיינה אוראלית נאותה, הכוללת צחצוח נכון פעמיים ביום ושימוש בחוט דנטלי לניקוי בין השיניים. החיידקים האוראליים חיים בפה כרובד ביופילם על השיניים, ולכן סילוק מכני על ידי צחצוח הוא הדרך היעילה ביותר להיפטר מהחיידקים הקריוגניים דוגמת S. mutans. אם יש צורך – הוספת מי פה ותכשירים עם חומרים ספציפיים הפעילים נגד החיידקים ומעכבים את שגשוגם יכולה לעזור, אך החיידקים בביופילם הרבה יותר עמידים בפני חומרים אנטי-חיידקיים או אנטיביוטיים. עם זאת, יש מספר חומרים יעילים ונפוצים אותם מוסיפים למוצרים הדנטליים השונים לשימוש בחלל הפה בנוסף לצחצוח[18].
חומרים אנטיבקטריאליים עריכה
דוגמאות לחומרים אנטי-בקטריאליים המשמשים בתכשירים שונים ברפואת שיניים (משחות שיניים, ג'ל לשימוש מקומי בפה ושטיפות פה):
- פלואוריד - חומר שלו השפעה מעכבת על האנזים אנולאז (אנזים המזרז שלב חיוני בתהליך הגליקוליזה). זאת בנוסף להשפעתו על עיכוב והיפוך הדה-מינרליזציה (השלב ההתחלתי של התהליך העששתי), לרה-מינרליזציה[19].
- כלורהקסידין (Chlorhexidine) - חומר הגורם להרג חיידקי S. mutans (וחיידקי פה נוספים) על ידי גרימת נזק לקרום תא החיידק. כלורהקסידין הוא חומר אנטי חיידקי בעל טווח פעולה רחב (נגד חיידקים גראם חיוביים, גראם שליליים, וגם נגד שמרים ונגיפים מסוימים). מנגנון הפעולה שלו קשור למבנהו הכימי: מכיוון שהוא טעון במטען חשמלי חיובי, הוא נספח לקרום התא של החיידקים (שלו מטען שלילי) ונקשר לפוספוליפידים שבו, דבר הגורם לנזקים לקרום התא ועקב כך לדליפת מרכיבים תוך תאיים החוצה. בריכוזים נמוכים הוא בקטריוסטטי (מעכב גידול חיידקים באופן הפיך), ובריכוזים גבוהים – בקטריוצידי (גורם להרג חיידקים) בגלל שקיעה בלתי הפיכה של הציטופלסמה[20][21].
בנוסף, לכלורהקסידין יש תכונות סובסטנטיביות – כלומר, הוא נספח לאתרים שונים בחלל הפה, וכך ממשיך להשפיע גם לאחר גמר השימוש בו[22].
-
המבנה הכימי של מולקולת כלורהקסידין
חיסון עריכה
מחקרים במעבדות ובמודלים של חיות הראו שחיסונים נגד מרכיבים שונים של mutans streptococci מדכאים התיישבות של החיידקים על השיניים במנגנונים שונים, וכך מפחיתים התפתחות עששת. ישנם מחקרים בחיות ובבני אדם לגבי שימוש ב"אנטיגן" I/II (הנקשר למרכיב גליקופרוטאיני של שכבת הרוק המצפה את השיניים), כגורם מחסן נגד החיידק S. mutans, ובכך נמנעת ההתיישבות (קולוניזציה) שלו על השיניים ותחילת התהליך העששתי[23]. בנוסף לעיכוב ההתיישבות על השיניים, לנוגדנים הנוצרים כנגד "אנטיגן" I/II יש השפעה נוספת - הם גם מעודדים הרג של החיידקים הקריוגניים על ידי נויטרופילים[1].
אסטרטגיות נוספות הקיימות למניעת התיישבות של S. mutans על השיניים (ודרך זה - מניעת עששת) כוללות: חיסון נגד גלוקוזיל טראנספראז (GTF=Glucosyl transferase) - האנזים המייצר גלוקנים דביקים מפירוק הסוכרים, וכן נגד החלבון הקושר גלוקנים (GbP=Glucan binding protein)[1]. גם בצורה זו משובשת היכולת של החיידקים להידבק זה לזה ולמשטחי השיניים. נבדקו סוגי חיסונים שונים בחיות ניסוי, כמו חלבונים שונים של החיידקים, או חיסונים המתבססים על רצפים של חומצות גרעין ועוד. עם זאת, לא קיימים כרגע בשוק חיסונים נגד עששת, מסיבות רבות - ביניהן אי יכולתם של החיסונים להשרות נוגדנים ברמה גבוהה מספיק להגנת חלל הפה[24].
ראו גם עריכה
לקריאה נוספת עריכה
- Oral microbiology and immunology. 2/e by Richard J. Lamont, George N. Hajishengallis, Howard F. Jenkinson. Publisher: ASM Press Washington DC . P. 229. ISBN 978-1-55581-673-5 (2014).
- Essental microbiology for dentistry. edited by Lakshman Samaranayake Publisher: Chuchill Livingstone Elsevier (2012).
קישורים חיצוניים עריכה
- Streptococcus mutans, באתר ITIS (באנגלית)
- Streptococcus mutans, באתר NCBI (באנגלית)
- Streptococcus mutans, באתר האנציקלופדיה של החיים (באנגלית)
- Streptococcus mutans, באתר GBIF (באנגלית)
הערות שוליים עריכה
- ^ 1 2 3 4 5 6 7 8 9 Oral microbiology and immunology. 2/e by Richard J. Lamont, George N. Hajishengallis, Howard F. Jenkinson. Publisher: ASM Press Washington DC (2014). P. 229-240. ISBN 978-1-55581-673-5
- ^ 1 2 3 Clarke JK. On the Bacterial Factor in the Ætiology of Dental Caries Br J Exp Pathol (1924); 5(3): 141–147. PMCID: PMC2047899
- ^ 1 2 Bratthall D. Demonstration of five serological groups of streptococcal strains resembling Streptococcus mutans. Odontologisk Revy (1970); 21(2):143-152
- ^ Loesche W J. Role of Streptococcus mutans in human dental decay. Microbiol Rev (1986); 50(4):353–380
- ^ Karpinski TM, Szkaradkiewicz AK. Microbiology of dental caries. J Biol Earth Sci (2013); 3(1): M21 -M24.
- ^ Ikeda T, Sandham HJ. Prevalence of Streptococcus mutans on various tooth surfaces in negro children. Arch Oral Biol (1971); 16 (10): 1237–40. doi:10.1016/0003-9969(71)90053-7. PMID 5289682 .
- ^ Selwitz RH, Ismail A I, Pitts N. B. Dental caries. Lancet (2007); 369(9555): 51-59
- ^ 1 2 Bowen, WH, Koo H. Biology of Streptococcus mutans-derived glucosyltransferases: role in extracellular matrix formation of cariogenic biofilms. Caries Res (2011); 45:69-86
- ^ Giertsen E, Arthur RA Guggenheim B. Effects of Xylitol on survival of mutans streptococci in mixed-six-species in vitro biofilms modelling supragingival plaque. Caries Res (2011);45:31–39DOI: 10.1159/000322646
- ^ Keyes PH. The infectious and transmissible nature of experimental dental caries. Archs Oral Biol (1960); 1:304-320
- ^ Hajishengallis G, Koga T, Russell MW. Affinity and Specificity of the Interactions between Streptococcus mutans Antigen 1/II and Salivary Components. J Dent Res (1994); 73(9):1493-1502
- ^ Berkowitz RJ, Turner J, Green P. Primary oral infection of infants with Streptococcus mutans. Archs oral Biol (1980); 25:221–224
- ^ Berkowitz RJ, Jordan HV, and White G. The early establishment of Streptococcus mutans in the mouth of infants (1975); Archs oral Biol 20:171–174
- ^ Duchin S, and Van Houte J, Colonization of teeth in humans by Streptococcus mutans as related to its concentrations in saliva and host age Infect Immun (1978); 20:120–125
- ^ Nakano K, Nomura R, Matsumoto M, Ooshima T. Roles of Oral Bacteria in Cardiovascular Diseases — From Molecular Mechanisms to Clinical Cases: Cell-Surface Structures of Novel Serotype k Streptococcus mutans Strains and Their Correlation to Virulence. J Pharmacol Sci (2010);113:120–125
- ^ Abranches J, Zeng L, Bélanger M, Rodrigues PH, Simpson- Haidaris PJ, Akin D, et al. Invasion of human coronary artery endothelial cells by Streptococcus mutans OMZ175. Oral Microbiol Immunol. 2009;24:141–145
- ^ Gold, OG, Jordan HV, and van Houte J. A selective medium for Streptococcus mutans. Arch. Oral Biol (1973); 18:1357-1364
- ^ Finkelstein P, Yost KG, Grossman E. "Mechanical devices versus antimicrobial rinses in plaque and gingivitis reduction". Clinical preventive dentistry (1990);12(3):8-11. PMID 2083478
- ^ Wiegand A, Wolfgang Buchalla W, Thomas Attin T. Review on fluoride-releasing restorative materials—Fluoride release and uptake characteristics, antibacterial activity and influence on caries formation. Dental Materials (2007); 23:343–362
- ^ Lin YH, Mickel AK, and Chogle S. Effectiveness of selected materials against Enterococcus faecalis: Part 3. The antibacterial effect of Calcium Hydroxide and Chlorhexidine on Enterococcus faecalis Journal of Endodntics (2003); 29(9):565-566
- ^ Jones C. Chlorhexidine: is it still the gold standard? Periodontology 2000 (1997); (15):55-62. Article first published online: 23 FEB 2007 DOI: 10.1111/j.1600-0757.1997.tb00105.x
- ^ Jenkins S, Addy M, Wade W. The mechanism of action of chlorhexidine. A study of plaque growth on enamel inserts in vivo. J Clin Periodontol (1988); 15(7):415–24. doi:10.1111/j.1600-051X.1988.tb01595.x. PMID 3183067
- ^ Russell MW, Childers NK, Michalek SM, Smith DJ, Taubman MA. A Caries Vaccine? The state of the science of immunization against dental caries. Caries research (2004); 38(3): 230–235. doi:10.1159/000077759. PMID 15153693
- ^ Smith DJ. Prospects in Caries Vaccine Development. J Dent Res (2012); 91(3):225-226